Mélanges de liquides


Le liquide est l’un des états de la matière. Dans la vie de tous les jours, le mélange de 2 liquides donne généralement une substance liquide.

Mélanger 6 liquides deux par deux. Observer et décrire les réactions.
Mettre 5 gouttes du liquide A au fond d’une éprouvette.
Rajouter 5 gouttes du liquide B.
Observer et noter dans un tableau.
Recommencer de façon à réaliser toutes les possibilités de mélanger les 6 liquides 2 par 2.

A
B
C
D
E
F
• 6 bouteilles contenant:
• Quelques éprouvettes
• Un porte-éprouvette


Buts de l'expérience
Matériel

Introduction

Méthode

Résultats

Remarques

Conclusions
Retour au portail des sciences



Retour au portail de chimie







Phénolphtaléine
Acide chlorhydrique 1N
Chlorure de calcium
Carbonate de sodium
Eau déionisée (déminéralisée)
Bleu de bromothymol

-
-
Liquide violet
-
Liquide jaune pâle
-
Apparition de bulles de gaz: réaction effervescente
-
Liquide jaune pâle
Apparition d’un solide : précipité blanc
-
Liquide bleu pâle
-
Liquide bleu foncé (de bromothymol)
Liquide bleu pâle
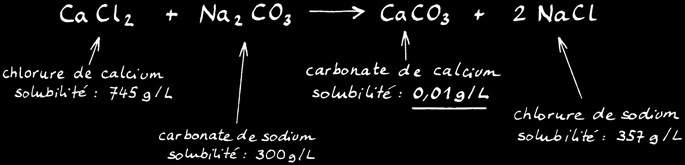
La réaction des liquides C+D donne un précipité blanc. La substance blanche qui trouble l’eau est la calcite qui est presque insoluble. Le “nuage” de calcite se forme selon la réaction:
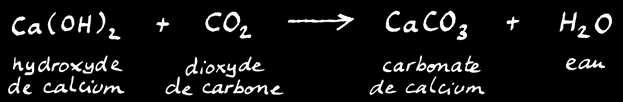
La faible solubilité du carbonate de calcium donne des idées pour mettre en évidence la présence de CO2 et même une façon de le pièger grâce à l’eau de chaux. L'hydroxyde de calcium (ou chaux éteinte) se dissout dans l'eau. Si on injecte du gaz carbonique (dioxyde de carbone) dans cette eau de chaux on a la réaction:
La faible solubilité de la calcite trahit immédiatement la présence du dioxyde de carbone: c’est une technique d’analyse simple.
•
•
•
•
A+B
A+C
A+D
A+E
A+F
B+C
B+D
B+E
B+F
C+D
C+E
C+F
D+E
D+F
E+F
Les liquides B + D réagissent par un dégagement de gaz: c’est une réaction effervescente . On note la réaction:
La réaction des liquides B + F donne un liquide bleu foncé. On comprend maintenant pourquoi ce liquide orange s’appelle bleu de bromothymol: il réagit au contact des liquides alcalins en changeant de couleur. De même il réagit avec les acides en prenant une couleur jaune. On l’utilise donc comme indicateur d’acidité.
1.
2.
C’est le dégagement de gaz carbonique ou dioxyde de carbone CO2 qu’on observe sous forme de bulles. Le produit de la réaction est une eau salée (NaCl) et effervescente.

3.
4.







