Les métaux







Ils sont d'excellents conducteurs électriques (ils conduisent l'électricité).








On reconnaît facilement les métaux grâce à leurs propriétés remarquables:
1.
Par leurs propriétés, les métaux ont été utilisés de multiples façons différentes:
4.
5.
La découverte et l'utilisation des métaux correspondent à de grandes époques de l'histoire de l'Humanité. On leur a donné les noms d'Ages du cuivre, du bronze, du fer.
Certains métaux ne sont faits que d'une seule sorte d'atomes: on dit que ce sont des corps purs. On les représente au moyen d’un symbole qu'on retrouve dans le tableau périodique des éléments (voir cours de chimie).
Exemples:
Le fer ( symbole: Fe ) n'est composé que d'atomes de fer.
L'aluminium ( Al ) n'est constitué que d'atomes d'aluminium.
Le cuivre ( Cu ) n'est composé que d'atomes de cuivre.
Propriétés des métaux
Les corps solides se dilatent lorsqu'ils reçoivent de la chaleur. Les métaux par exemples, très bons conducteurs électriques et thermiques, se dilatent fortement lorsqu'ils emmagasinent de la chaleur.
Un rail en acier mesure 15 m de longueur à 0°C. Quelle est sa longueur à 40°C?
Un pont métallique (acier) mesure 60 m de longueur à 0°C. En hiver, la température descend jusqu'à -20°C; en été elle peut atteindre +40°C. Entre quelles valeurs la longueur du pont peut-elle varier au cours de l'année?
Un fil de fer a une longueur de 3 km à la température de 40°C. Quelle est sa longueur à -30°C?
Un fil de cuivre a une longueur de 1 km à la température de 20°C. Quelle doit être sa température pour qu'il s'allonge de 10 cm?
Une tige de cuivre a une longueur de 1 m à la température de 20°C. On veut fixer bout à bout deux tiges, l'une de fer, l'autre de plomb, de manière que la tige composée ait à toute température la même longueur que la tige de cuivre. Quelles doivent être les longueurs des tiges de fer et de plomb?
Deux tiges métalliques, l'une de cuivre, l'autre de fer sont soudées à une extrémité et placées l'une à côté de l'autre. Quelles doivent être les longueurs de ces tiges à 0°C si l'on veut que la distance entre les extrémités libres soit indépendante de la température et vaille 20 cm?
Ils sont, mis à part les métaux nobles comme l'or, oxydables (facilement attaqués par l'oxygène et d'autres substances). Il se forme alors en surface une couche d'oxyde ("rouille"): les métaux perdent leur éclat et finissent par se faire ronger. On peut les protéger par une couche de peinture, d'huile ou de graisse.
On peut mélanger différents métaux pour faire des alliages qui ont des propriétés nouvelles: ils peuvent être plus résistants, moins malléables, moins lourds, inox (inoxydables), supraconducteurs (laissent passer le courant électrique sans résistance), etc...
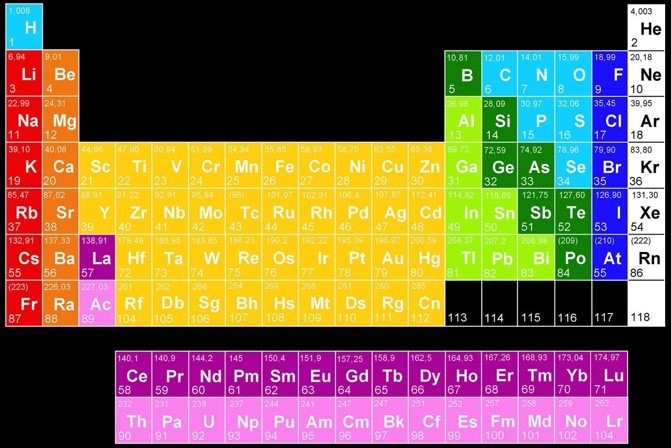










Métaux alcalins
Métaux alcalino-terreux
Métaux de transition
Lanthanides
Actinides
Métaux pauvres
Métalloïdes
Non-métaux
Halogènes
Gaz rares
Les métaux sont caractérisés par leur tendance à donner des électrons. Ce qui explique leur sensibilité à l’oxydation, à la corrosion. Dans le tableau périodique des éléments, on range les métaux à gauche et les non-métaux à droite. Les éléments “métalloïdes” ont des propriétés intermédiaires.

Joint de dilatation sur l’autoroute A9, viaduc de Chillon

Bronze, pointe de lance
5e siècle avant JC , Olympie




Utilisation des métaux

Histoire des métaux

Métaux et non-métaux

Dilatation et contraction
7.
8.

Fer, heaume
1400 , Milan

Les métaux purs
Acier: alliage fer (Fe) + carbone (C). La masse de carbone représente moins de 2 %.
Acier inoxydable : alliage fer + carbone + chrome + nickel, ...
Fonte: alliage fer + carbone. La masse de carbone est comprise entre 2 et 6 %.
Bronze (ou 'airain') : alliage + cuivre (Cu) + étain (Sn).
Laiton : alliage cuivre (Cu) + zinc (Zn)
Lorsqu'on mélange divers métaux à l'état liquide et qu'on les refroidit: on obtient de nouveaux métaux qu'on appelle alliages. Ils sont faits de plusieurs sortes d'atomes mélangés en différentes proportions.
Exemples:

Les alliages
français
Acier
Aluminium
Argent
Bronze (airain)
Chrome
Cobalt
Cuivre
Etain
Fer
Fonte
Laiton
Nickel
Or
Plomb
Potassium
Sodium
Zinc
Le fer blanc ou fer étamé est recouvert d’une couche d’étain pour le protéger de l’oxydation
symbole
chimique
-
Al
Ag
-
Cr
Co
Cu
Sn
Fe
-
-
Ni
Au
Pb
K
Na
Zn
anglais
steel
aluminium
silver
bronze
chromum
cobalt
copper
tin
iron
cast iron
brass
nickel
gold
lead
potassium
sodium
zinc
allemand
stahl
aluminium
silber
bronze
chrom
kobalt
kupfer
zinn
eisen
gusseisen
messing
nickel
gold
blei
kalium
natrium
zinc
latin
-
-
argentum
-
-
-
cuprum (de Chypre)
stannum
ferrum
-
-
-
aurum
plumbum
-
-
-
L’acier n’a pas de symbole chimique. Pourquoi?
Il n’était pas encore connu lors de la découverte du tableau périodique
Ce n’est pas un corps pur mais un alliage.
C’est une substance qui n’existe pas dans la nature.
•
•
•
•
•
•

On peut trouver dans la nature des métaux purs: les métaux natifs. Ce sont les métaux nobles: l'or, l'argent et le cuivre qui ont pu résister à l'attaque des éléments oxydants tels que l'oxygène, le fluor, le chlore et le soufre.

cuivre natif

les parties vertes correspondent à du cuivre oxydé
Minerai de cuivre (Congo) formé de carbonate et d’hydroxyde de cuivre CuCO3 . Cu(OH)2
Ce minéral de couleur verte s’appelle malachite.
La métallurgie consiste à séparer les constituants des minerais afin d'extraire les différents métaux utiles à l'industrie humaine.
Sur Terre on trouve généralement les métaux sous forme de minerais: les métaux sont alors combinés avec des éléments oxydants et forment des oxydes, des hydroxydes, des chlorures, des sulfures,...



Minerai de fer (Itabira, Brésil).

Minerai d’aluminium ou bauxite
(lac de Carcès, France).


Métaux et minerais
On trouve du fer natif dans les météorites ferreuses car elles ont été formées à l'abri de l'oxygène. Mais une fois tombées sur Terre, elles rouillent rapidement.


tranche de météorite ferreuse (Namibie)

Aluminium, cafetière
1933 , Italie

Cuivre natif,
Michigan, USA


cuivre
zinc
laiton
+
=

hélice et saxophone en laiton

•
•
•
•
•

Maillechort (couronne de la pièce)
cuivre + zinc + nickel (75 % Cu _ 20 % Zn_5 % Ni)
Cupronickel (coeur de la pièce)
alliage cuivre + nickel (75 % Cu _ 25 % Ni)














Or, pièce de Constantin,
350 ap. J-C.



1.
2.
3.
4.
5.
6.


Métal et monnaie


or
Suisse 20 CHF
Vreneli 1997
Au90%Cu10%
argent
Suisse 1 CHF
1943
Ag835Ag83,5%_Cu16,5%
aluminium
France5 FF
1945
Al
bronze
France10 centimes
1854
Napoléon III second Empire


On appelle coefficient de dilatation linéaire d'un corps solide, l'allongement que subit l'unité de longueur (1m) de ce corps lorsque sa température s'élève de 1°C.
Le coefficient linéaire de l'acier est de 0,00001, ce qui signifie qu'une tige d'acier d'un mètre s'allonge de 0,00001m (ou 0,01 mm) pour une élévation de température de 1°C.
Définition:
Exemple:
Certains métaux se dilatent plus que d'autres. L'aluminium s'allonge deux fois plus sous l'effet de la chaleur que l'acier par exemple.
L'allongement d'une tige dépend de l'élévation de température et de la nature du corps.



Ils sont fusibles: on peut les fondre (et mouler des objets).
6.

Ils sont ductiles (on peut les étirer en fils).
5.
Ils sont malléables (on peut les tordre sans les casser).
4.
Ils ont un éclat métallique (ils brillent).
3.
Ils sont d'excellents conducteurs thermiques (ils conduisent la chaleur).
2.
Comme moyen d'échange (monnaie): or, argent,...
1.
Pour faire des bijoux : l'or brille et ne s'oxyde pas.
2.
Comme moyen de communication (fils électriques).
Comme source d’énergie: l'uranium (U) est un “combustible” nucléaire.
Pour faire des outils: le métal se coule dans un moule et prend sa forme.
3.







Cupronickel : alliage cuivre + nickel (75 % Cu _ 25 % Ni)
Maillechort (ou 'argentan'): cuivre + zinc + nickel (75 % Cu _ 20 % Zn_5 % Ni)
•
•
Alliages d'aluminium (léger)
Alliage plomb-étain : pour la brasure.
Ruolz : nickel + argent + cuivre
Invar : se dilate peu (63,5 % Fe_ 36 % Ni_ 0,4 % Mn_ 0,1 % C).
Une foule d'alliages à base de Ni, Cr, Ti, Al, Mg, V, ...
•
•
•
•
•


Fin de la page
Retour au portail du corps humain




Retour au portail de physique


Retour au cours de géologie


Retour au cours d’astronomie
Retour au portail des sciences




Retour au cours de chimie









Elle est entourée d’une gangue de fluorine CaF2
Mine des Trappistes, Valais (Suisse)
La galène est un sulfure de plomb (PbS).



Métal_monnaie
Métal_7e
nickel
plomb
étain
aluminium
cuivre
zinc
fonte
laiton









Collection métaux






